Grafiet, molekulêre formule: C, molekulêre gewig: 12.01, is 'n vorm van element koolstof, elke koolstofatoom word verbind deur drie ander koolstofatome (gerangskik in heuningkoek seshoeke) om 'n kovalente molekule te vorm. Omdat elke koolstofatoom 'n elektron uitstraal, dié wat vrylik kan beweeg, dus is grafiet 'n geleier.
Grafiet is een van die sagste minerale, en die gebruike daarvan sluit in die maak van potloodleidrade en smeermiddels. Koolstof is 'n nie-metaalelement wat in die tweede siklus IVA-groep van die periodieke tabel geleë is. Grafiet word by hoë temperature gevorm.
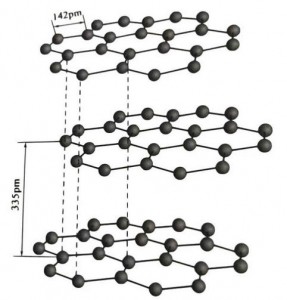
Grafiet is 'n kristallyne mineraal van koolstofelemente, en sy kristallyne rooster is 'n seskantige gelaagde struktuur. Die afstand tussen elke maaslaag is 3,35A, en die spasiëring van koolstofatome in dieselfde maaslaag is 1,42A. Dit is 'n seskantige kristalstelsel met 'n volledige gelaagde splitsing. Die splitsingsoppervlak is hoofsaaklik molekulêre bindings, minder aantreklik vir molekules, so sy natuurlike dryf is baie goed.
In grafietkristalle vorm die koolstofatome in dieselfde laag 'n kovalente binding met sp2-hibridisasie, en elke koolstofatoom is in drie kovalente bindings aan drie ander atome verbind. Die ses koolstofatome vorm 'n ses-aaneenlopende ring in dieselfde vlak, wat strek tot in 'n lamelstruktuur, waar die bindingslengte van die CC-binding 142pm is, wat presies binne die bindingslengtereeks van die atoomkristal is, dus vir dieselfde laag , dit is 'n atoomkristal. Koolstofatome in dieselfde vlak het een p-baan, wat mekaar oorvleuel. Elektrone is relatief vry, gelykstaande aan vrye elektrone in metale, dus kan grafiet hitte en elektrisiteit gelei, wat die kenmerk van metaalkristalle is. So ook geklassifiseer as metaalkristalle.
Die middelste laag grafietkristal word deur 335pm geskei, en die afstand is groot. Dit word gekombineer met van der Waals-krag, dit wil sê die laag behoort aan die molekulêre kristal. Omdat die binding van koolstofatome in dieselfde vlakke laag egter baie sterk en uiters moeilik is om te vernietig, is die oplospunt van grafiet ook baie hoog en is die chemiese eienskappe daarvan stabiel.
In die lig van sy spesiale bindingsmodus, kan nie as 'n enkele kristal of polikristal beskou word nie, word grafiet nou algemeen beskou as 'n gemengde kristal.
Plaas tyd: Jul-31-2023